 5588
5588 5588
5588Богатая тромбоцитами плазма (БоТП, PRP) используется во многих областях медицины из-за доказанного положительного воздействия на трофику тканей.
БоТП применяется и изучается с 1970-х гг. и внедрена в стандартную клиническую практику в дерматологии, пластической хирургии, стоматологии, ортопедии, акушерстве и гинекологии1.
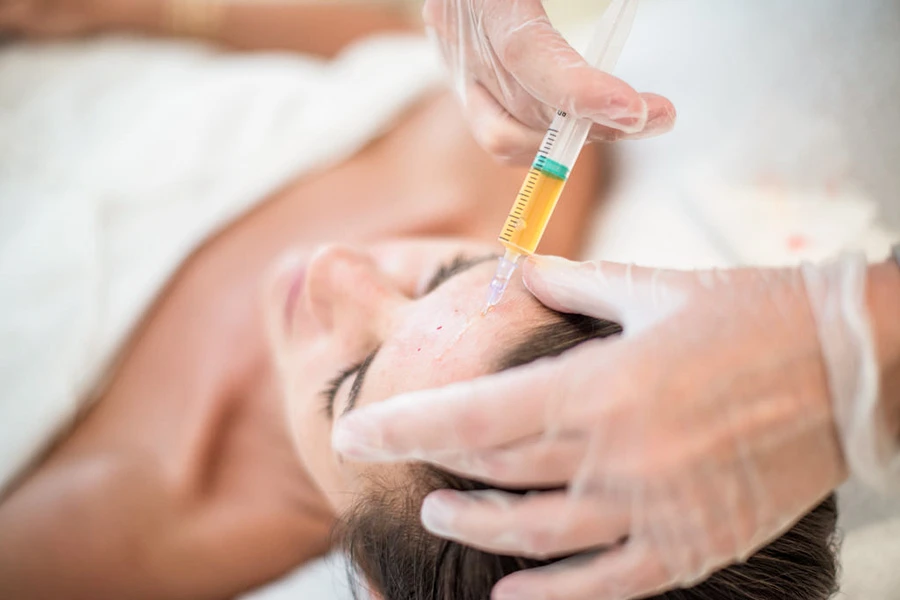
В регенеративной медицине БоТП используется с момента установления ее эффективности при регенерации тканей2. Ее широкое применение обусловлено доступностью, аутологичным характером, исключающим иммунный ответ, легкостью использования, низкой стоимостью по сравнению с другими методами регенеративной медицины. В дерматологии и косметологии PRP используется для лечения акне, рубцов и алопеции (особенно у женщин)3. Она также эффективна для омоложения кожи лица, подтяжки кожи вокруг глаз, как подготовительный этап перед сложными процедурами (аппаратные методики), а также в качестве посттерапии.
БоТП представляет собой плазму с высоким содержанием тромбоцитов, получаемую посредством центрифугирования периферической крови4.
Тромбоциты несут в себе более 800 видов белковых молекул, цитокинов, гормонов и хемоаттрактантов5 и содержат три вида гранул: альфа-гранулы, плотные гранулы и лизосомы6. Активация тромбоцитов индуцирует выпуск различных биологически активных белков, стимулирующих пролиферацию, рост и дифференцировку клеток7. Выпускаемые активированными тромбоцитами биологически активные медиаторы включают в себя тромбоцитарный фактор роста (ТФР), трансформирующий ростовой фактор бета (ТРФ-β), фактор роста фибробластов (ФРФ), эпидермальный фактор роста (ЭФР), инсулиноподобный фактор роста 1 (ИФР-1) и фактор роста гепатоцитов (ФРГ).
Эти факторы роста модулируют пролиферацию, дифференцирование, ангиогенез и хемотаксис клеток, анаболизм, контролируют воспалительный процесс8.
Когда БоТП посредством крошечных проколов вводится в поврежденную область, она стимулирует ткань, вызывая легкое воспаление, которое запускает каскад заживления. В результате начинает вырабатываться новый коллаген. По мере созревания этот коллаген начинает сжиматься, подтягивать и укреплять кожу9.
Ключевые факторы успешного применения БоТП:
Сегодня врачам доступно множество готовых наборов для проведения плазмотерапии, имеющих различные системы сепарации БоТП.
Различие между ними заключается в содержании тромбоцитов, лейкоцитов и факторов роста в конечном препарате, их разделении, а также в стерильности10.
Разным системам для работы требуется разный объем крови, при этом при заборе он не всегда коррелирует с количеством получаемых тромбоцитов.
Исследования показывают, что в идеале БоТП должна содержать в 4–7 раз больше тромбоцитов, чем циркулирующая кровь11. Помимо количества тромбоцитов, на степень противовоспалительного эффекта и терапевтическую успешность инъекций БоТП влияют количество мононуклеарных клеток, нейтрофилов и эритроцитов12.
Во избежание развития воспаления предпочтительно использовать также препараты, содержащие исключительно тромбоциты, без нейтрофилов и эритроцитов13.
Недавно в России появились наборы для плазмотерапии T-LAB от турецкой компании T-Biotechnology Laboratory (Стамбул, Турция; сертификат РУ № РЗН 2020/12523).
Теоретические разработки, лежащие в основе производства T-LAB, были признаны в числе лидеров отрасли исследовательским центром Grand View Research Company (Сан-Франциско), а в 2018 году компания была номинирована на премию «Глобальный рынок PRP» наряду с восемью другими мировыми производителями.
Все производственные процессы выполняются в рамках системы качества ISO 13485, производство пробирок соответствует международному стандарту ISO 8.
Компания более десяти лет проводит испытания своих наборов.
Эффективность пробирок T-LAB подтверждена в ряде исследований Mishra et al.14, которые показали, что набор обеспечивает в 4,75 раза более высокую концентрацию тромбоцитов по сравнению с кровью. В исследовании две пробирки по 10 мл из набора центрифугировали при 1500 x g в течение 8 минут, и было получено 4 мл БоТП.
Расчеты, выполненные посредством сопоставления содержания тромбоцитов, красных кровяных телец и лейкоцитов с учетом объема собранной крови и полученной БоТП, показали, что набор компании T-LAB позволяет посредством центрифугирования с рекомендованными производителем параметрами получать БоТП в объеме больше среднего (4,5 мл) относительно других изделий.
Коэффициент соотношения концентрации лейкоцитов к тромбоцитам соответствует одним из наименьших значений, зафиксированных в доступной литературе, что позволяет определить получаемую с помощью набора T-LAB БоТП как обедненную лейкоцитами15.
Еще одним важным аспектом применения БоТП является получение стерильного препарата. Методы работы с БоТП вручную могут создавать угрозу бактериального загрязнения при получении препарата16. В большинстве продуктов не содержится антикоагулянт, а потому его требуется добавлять.
Наборы Т-LAB содержат антикоагулянт на основе цитрата натрия, что исключает риск загрязнения. Тесты показали, что изделия T-LAB позволяют достигать чистоты > 90 %; лишь 7 из 36 описанных в существующей литературе изделий характеризуются схожими показателями.