Актуальность лечения себорейного дерматита и акне неоспорима: данные патологии встречаются часто – у 60–80 % лиц в возрасте 12–35 лет, они снижают самооценку больных, у которых возникают сложности в адаптации в социальной и интимной сфере. 30% подростков и 5 % взрослых нуждаются в активной психолого-психиатрической помощи1.
Лечение больных себореей и акне всегда комплексное и включает патогенетическую терапию и адекватный домашний уход за кожей. На сегодняшний день известно, что терапия ботулиническим токсином типа А (БТА) является эффективным и безопасным методом лечения розацеа3, себорейного дерматита и акне.
Жирность кожи связана с производством кожного сала сальными железами5. Гиперпродукция и дисбаланс липидов секрета гиперплазированной сальной железой – это одно из основных звеньев патогенеза акне6.
Деятельность сальных желез регулируется в основном гормональными механизмами. Также на количество вырабатываемого кожного сала (себума) влияют состав и количество потребляемой пищи, возраст, пол и время года7, 9, 10. Уровень секреции кожного сала максимален в возрасте от 15 до 35 лет, затем она снижается. Как правило, секреция кожного сала у мужчин значительно выше, чем у женщин11,12.
Резюмируя, можно сказать, что все эти факторы могут объяснить вариабельность показателей выработки кожного сала.
Большинство терапевтических подходов, используемых для лечения себорейного дерматита и акне, имеют различную степень эффективности и включают системные препараты, такие как изотретиноин, антибиотикотерапию и гормональные препараты, а также местные препараты, такие как наружные ретиноиды, азелаиновая кислота, бензоила пероксид16. Кроме того, для лечения жирной кожи используется фотодинамическая терапия и лазерные системы. Однако большинство этих методик имеют серьезные побочные эффекты, такие как тератогенность (изотретиноин), тромбофлебиты, «прорывные» кровотечения, тошнота, болезненность молочных желез (оральные контрацептивы), сухость и контактный дерматит (наружные ретиноиды, азелаиновая кислота, бензоила пероксид) и др.17
В 2002 году FDA одобрило ботулинический токсин для использования в косметологии.
В последнее время БТА стали применять для лечения розацеа, рубцов, акне и жирной кожи19. Одно из первых сообщений в литературе, где упоминается потенциал для улучшения качества жирной кожи при использовании ботулинического токсина, появилось в 2008 году.
Механизм действия БТA, способствующий снижению выработки кожного сала, до конца не установлен.
Известно, что ботулинический токсин расщепляет белки, участвующие в слиянии синоптического пузырька с плазматической мембраной пресинаптического нейрона терминального аксона. Данные пузырьки содержат нейромедиатор ацетилхолин. БТА блокирует высвобождение этого нейромедиатора в синаптическую щель, где обычно происходит его прикрепление к мускариновым рецепторам на постсинаптических клетках. В сальных железах находятся незрелые и зрелые себоциты, экспрессирующие мускариновые ацетилхолиновые рецепторы, которые важны для дифференцировки себоцитов и, как следствие, для выработки кожного сала20, 21, 22. Ли и соавторы предположили, что БТA эффективно снижает выработку кожного сала за счет блокады холинергических синапсов. Также автор сообщает, что люди с жирной кожей более чувствительны к ацетилхолину (АХ), чем люди с нормальной кожей, т. к. они имеют большее количество зрелых себоцитов и большее количество АХ. Данная теория подтвердилась на практике, исследования показали, что внутрикожные инъекции ботулинического токсина значительно уменьшили себорею у лиц с жирной кожей, но не повлияли на себосекрецию у людей с нормальной кожей15, 23.
Другая версия основана на том, что чаще всего сальная железа располагается между волосяным фолликулом и мышцей, поднимающей волос, последняя стимулируется адреналином и симпатической нервной системой. Роуз и Голдберг предположили, что внутрикожные инъекции БТA снижают экскрецию кожного сала за счет нейромодулирующего эффекта БТA на мышцу, поднимающую волос24.
Следовательно, можно предположить, что БТA эффективно снижает выработку кожного сала за счет блокады холинергической передачи сигнала и нейромодулирующего эффекта БТА на мышцу, поднимающую волос, но для более детального понимания данного механизма необходимы дальнейшие исследования.
Кроме того, ботулотоксин также способствует подавлению нейрогенного воспаления. БТА блокирует транспортные белки, участвующие в высвобождении воспалительных нейромедиаторов в терминалях сенсорных нервов25, 26: субстанцию Р, кальцитонин-генсвязанный пептид, нейрокинин. Таким образом, можно предположить наличие противовоспалительного действия БТА при акне.

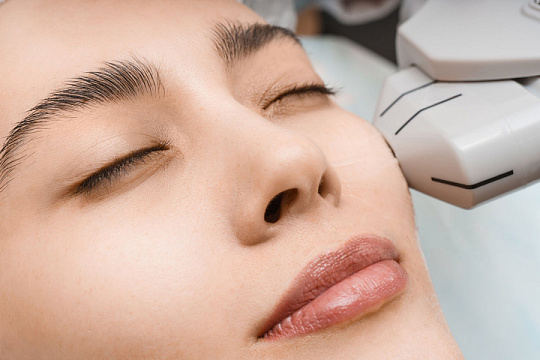
Рис. 1. Разметка пациентки перед проведением процедуры.
Обоснование исследования: Жирная кожа является одной из наиболее распространенных дерматологических жалоб на приеме у врача-дерматолога, косметолога. Пациенты с жирной себореей также отмечают расширение пор, акне и другие косметические проблемы.
Цель исследования: Оценка эффективности инкоботулотоксина А (инкоБТА) (Ксеомин, Merz Pharmaceuticals GmbH) при лечении угревой болезни (акне).
Тип исследования: проспективное.
Место проведения: клиника Марии Ширшаковой, Москва, сентябрь - октябрь 2018 года.
В исследование включены 12 участников: 10 женщин, средний возраст которых составил 26 лет, и 2 мужчины, средний возраст – 29 лет. В своем исследовании для оценки степени тяжести акне использовалась классификация Американской академии дерматологии (приводится в российской модификации):
У женщин преобладала I степень тяжести угревой болезни (у 90 %), 5 % имели II степень и оставшиеся 5 % – III степень тяжести угревой болезни соответственно. Среди мужчин – один пациент (50 %) имел I степень тяжести акне, у другого (50 %) была выявлена II степень тяжести акне. Также у 70 % женщин и у 100 % мужчин наблюдались следы постакне (рубцы).
Дизайн исследования: Всем пациентам использовалась одинаковая схема инъецирования. Дозировки инкоботулотоксина типа А варьировали от 6 до 8 ЕД на одну область введения в зависимости от пола.
Использовался препарат 100 ЕД в разведении 1:4 с 0,9 % раствором хлорида натрия. Препарат Ксеомин вводился мультифокальной внутрикожной техникой равномерно по всей зоне лица. Всем пациентам проводилась аппликационная анестезия.
Затем выполнялась разметка лица. Препарат вводился из расчета 0,25 ЕД/см2 или 0,125 ЕД/0,5 см2.
На время исследования исключалось применение системных и местных средств для лечения угревой болезни.
Методика: Всем пациентам проводилась разметка на квадранты, вертикальные линии, проведенные по срединной линии лица, через головку, талию и хвост бровей перпендикулярно к линии нижней челюсти, а также вертикальные линии две в области лба – срединная и на 3 см выше бровей, а также линию, соединяющую козелок и крыло носа, мочку уха и угол рта, делящие зоны лица на квадраты (Рис. 1). В каждый квадрат вводилось 0,125–0,25 ЕД Ксеомина внутрикожно.
У 100 % пациентов отмечен выраженный эффект от терапии.
Фиксировались положительные эффекты от терапии:
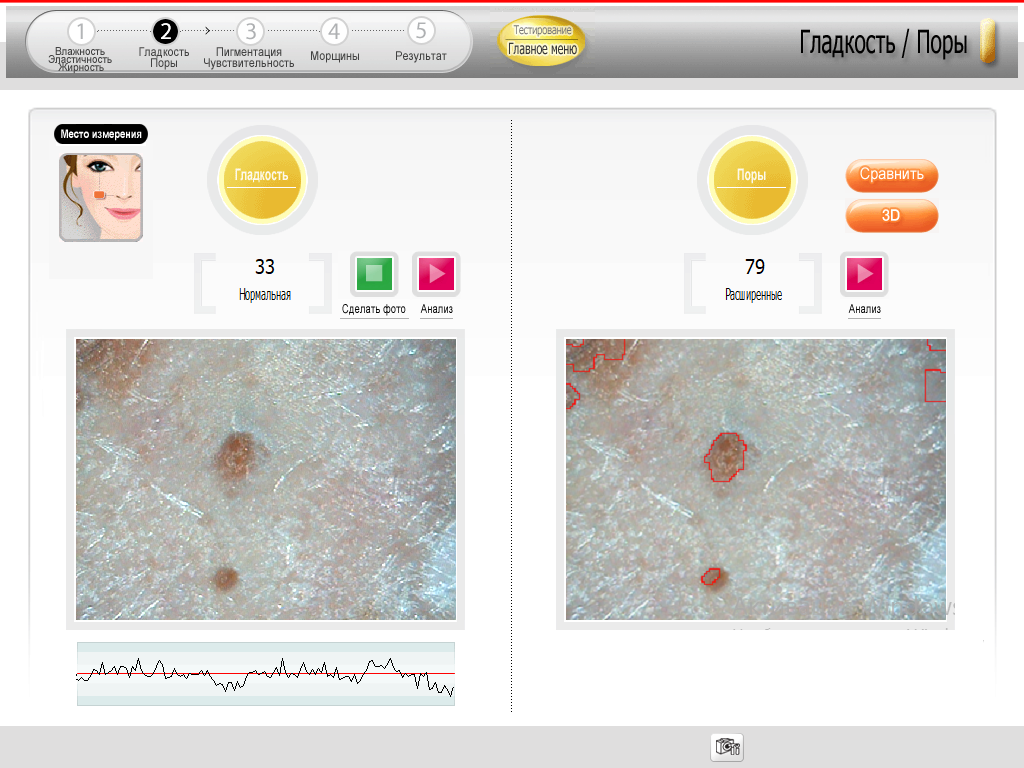
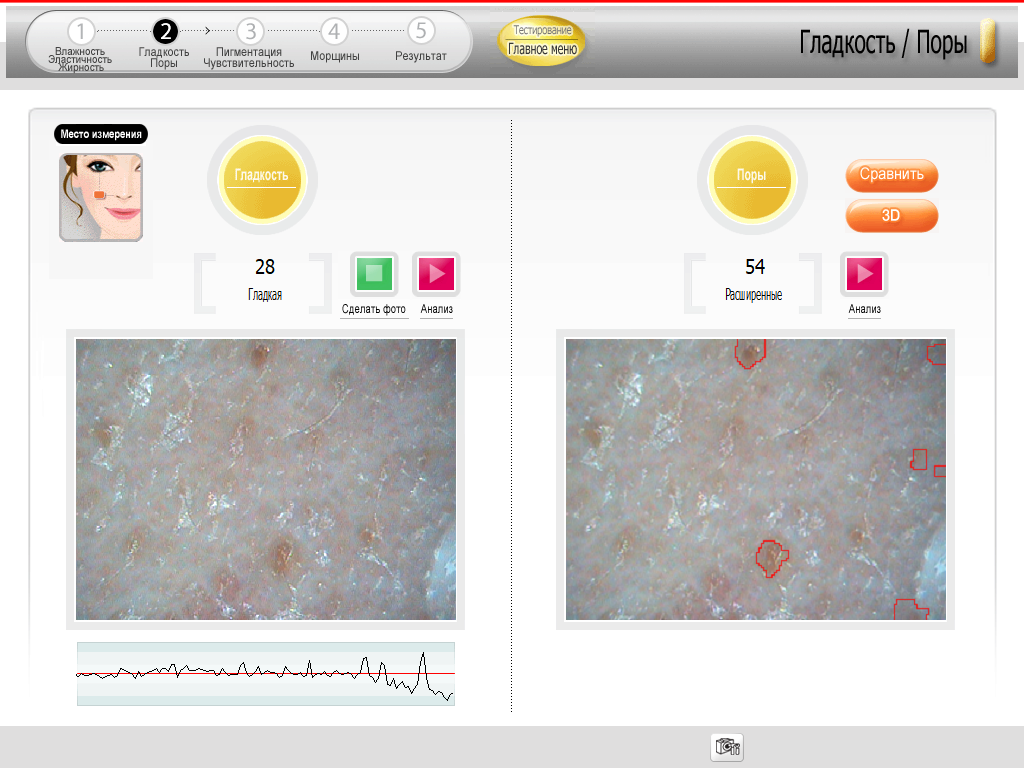
Выраженное сужение пор (на 18 %) было подтверждено с помощью двухкратного измерения ширины и количества пор прибором дерматоскоп Арамо SG и программой SkinXPрro с интервалом в 14 дней (Рис. 2).
Также при помощи специально проводимых проб оценивалась жирность кожи, и у всех пациентов мы наблюдали значимое снижение (на 40 %) показателей салоотделения как в Т-зоне, так и в других областях.
В результате терапии у пациентов наблюдалось также сглаживание рельефа кожи (на 16 %), небольшое разглаживание мимических морщин (на 14 %). Значительных побочных эффектов от проводимой терапии не отмечалось.

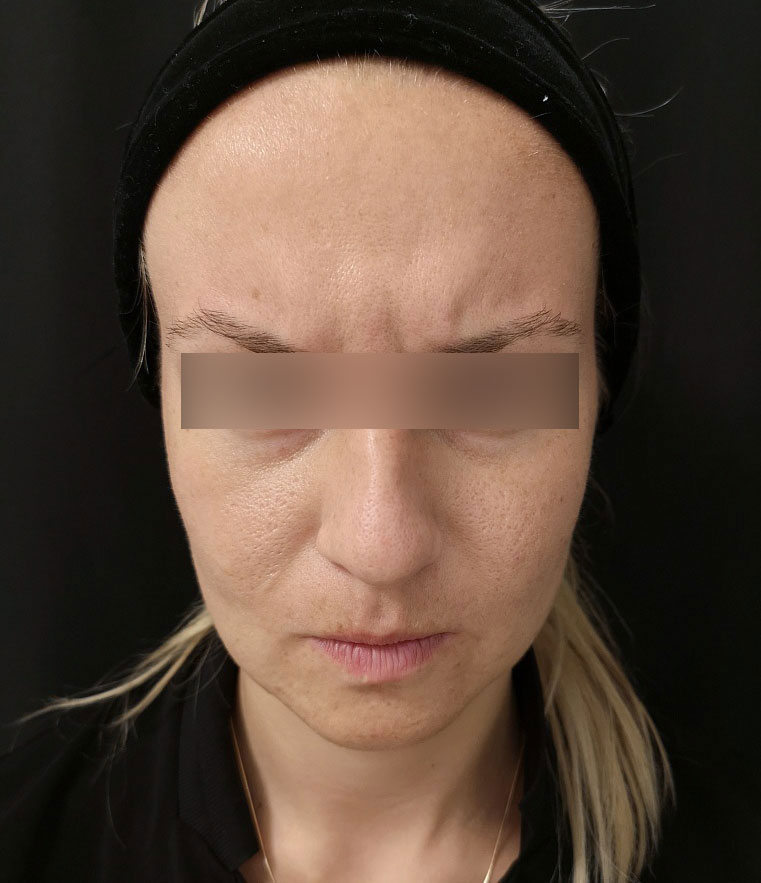
Пациентка, 32 года. До лечения Ксеомином. Фото предоставлены Ширшаковой М.А.

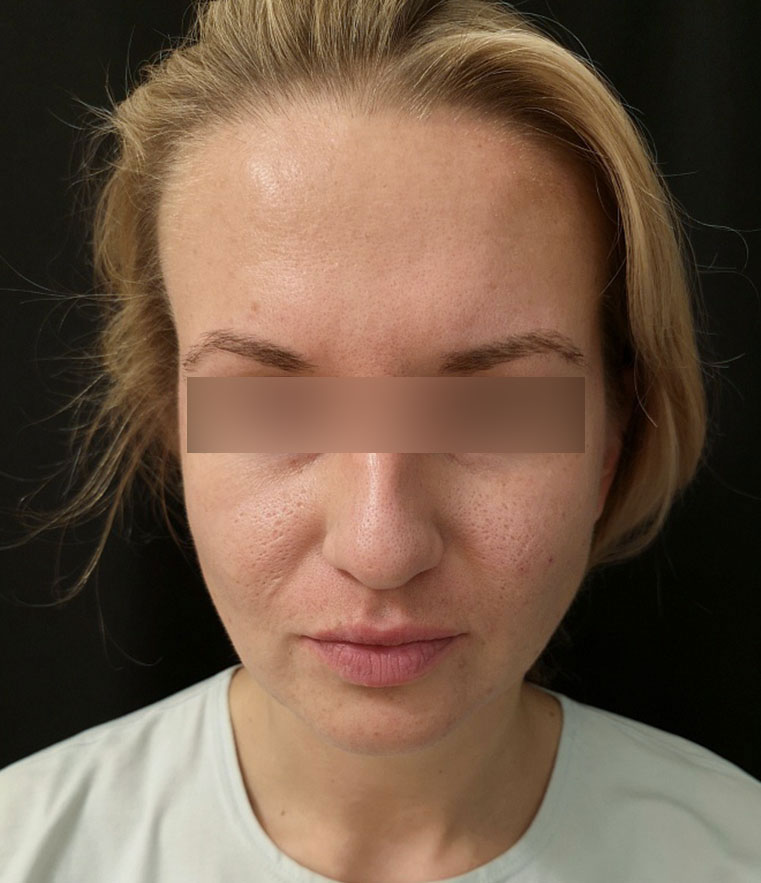
Пациентка, 32 года. После лечения Ксеомином. Фото предоставлены Ширшаковой М.А.
Пациентка, 28 лет. До лечения Ксеомином. Фото предоставлены Ширшаковой М.А.
Пациентка, 28 лет. После лечения Ксеомином. Фото предоставлены Ширшаковой М.А.
Исследование показало, что внутрикожные инъекции инкоБТА Ксеомина снижают выработку кожного сала на 40 % и размер пор на 18 %, также выравнивают рельеф кожи, «сглаживают» рубцы постакне на 16 %. Кроме того, удовлетворенность пациентов после процедуры была высокой, и значительных побочных эффектов не наблюдалось. БТA эффективно снижает выработку и выделение кожного сала, и, основываясь на литературных данных, это снижение могло быть достигнуто посредством блокады холинергической передачи сигналов и нейромодулирующего эффекта БТA на мышцу, поднимающую волос.
Внутрикожные инъекции инкоботулотоксина могут представлять собой новый, многообещающий метод лечения акне, жирной кожи и симптомокомплекса постакне.


Комментарии