Метод «разведения филлера» завоевал популярность среди врачей-косметологов, его используют, чтобы изменить реологические характеристики препаратов, сделать их универсальными и получить экономическую выгоду. Но разные препараты при разведении ведут себя по-разному. В новом американском исследовании при поддержке «Мерц Эстетикс» Алекс Маккарти, доктор наук, эксперт по регенеративной медицине, и другие ученые провели анализ реологических характеристик препарата на основе CaHA-КМЦ в различных разведениях и других популярных дермальных филлеров и биостимулирующих препаратов. Главный вывод: Radiesse в разведении более 1:1 ведет себя подобно жидкости и может применяться для регенеративной биостимуляции, тогда как в стандартном состоянии он подобен гелю, который оказывает волюмизирующий эффект. 1nep.ru подготовил конспект научной статьи.
Из-за высокой стоимости и большого количества представленных на рынке дермальных филлеров врач-косметологи задаются вопросом: можно ли оптимизировать применение препарата с помощью разведения, так, чтобы повысить универсальность и экономическую эффективность? Метод «разведения» уже завоевал популярность среди практикующих специалистов, о чем свидетельствуют результаты опроса 2019 года среди почти 500 дерматологов. При этом основная цель использования этого метода — изменение реологических характеристик препаратов.
Среди множества реологических показателей самые информативные — комплексный модуль (G*), модуль упругости (Gʹ), модуль вязкости (G″) и коэффициент потерь tan δ: именно они характеризуют свойства филлера, связанные с определенными физическими свойствами (когезивность, прочность и пластичность). При прочих равных условиях более высокое значение G* означает, что гель более «плотный» и устойчивый к деформации, то есть обладает более высокой прочностью или когезивностью.
Гель, обладающий высокой упругостью, восстанавливает свою первоначальную форму, подобно пружине, преобразуя накопленную энергию приложенного напряжения обратно в кинетическую энергию и возвращаясь к своей первоначальной форме. Такие свойства измеряются модулем упругости при сдвиге Gʹ, который определяет количество накапливаемой энергии упругой деформации. Если остальные параметры одинаковы, более высокое значение Gʹ означает, что гель является более «упругим» или «эластичным» при надавливании, как жевательный мармелад. Напротив, гель, обладающий высокой вязкостью, остается деформированным после снятия приложенного напряжения. Такие вязкие или пластичные свойства геля, описываемые модулем вязкости при сдвиге G″, отражают способность материала рассеивать энергию, подобно амортизатору. При прочих равных условиях более высокое значение G″ означает, что гель более пластичный, вязкий или деформируется при надавливании, как мягкие ириски. Зависимость между G*, Gʹ и G″ свидетельствует о том, что эти модули всегда следует рассматривать во взаимосвязи при оценке свойств вязкоупругих материалов.
Зависимость между Gʹ и G″ удобно выражать в виде отношения G″/Gʹ, которое называется коэффициентом потерь или tan δ и позволяет прогнозировать свойства препарата. Для вязкоупругих твердых материалов, включая большинство дермальных филлеров в форме геля, значения tan δ находятся в диапазоне 0–1. Низкое значение tan δ (например, tan δ = 0,1) указывает на то, что модуль упругости в 10 раз превосходит модуль вязкости; благодаря преобладанию упругих свойств, гель устойчив к постоянной деформации.
В клинической практике выбор дермальных филлеров должен основываться на их реологических характеристиках с учетом плотности тканей в зоне введения и ожидаемого результата:
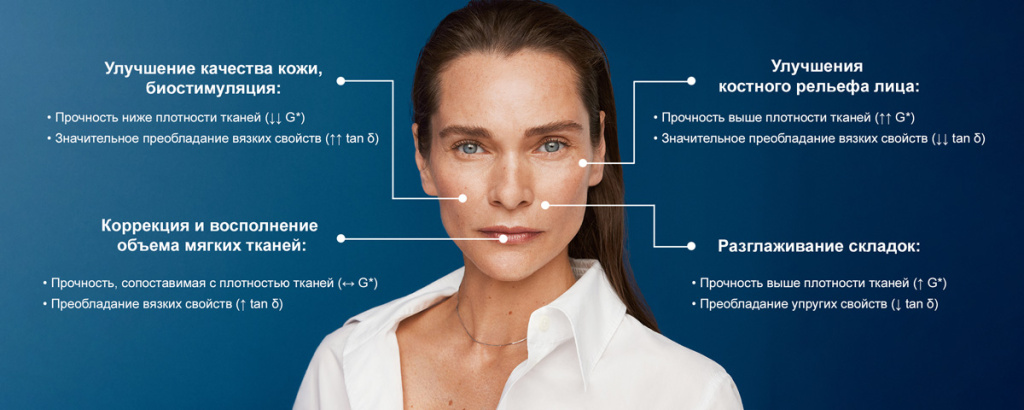
В одном из последних исследований были изучены реологические свойства препарата на основе кальция гидроксиапатита и карбоксиметилцеллюлозы (CaHA-КМЦ) (Radiesse®, производитель «Мерц Эстетикс») в высоком разведении. Данные реометрии свидетельствуют о том, что можно изменять реологический профиль гелей на основе CaHA-КМЦ с учетом индивидуальных потребностей пациентов в континууме «упругость–регенерация» с высокой эластичностью/упругостью, прямым волюмизирующим эффектом с одной стороны и низкой когезивностью, биостимулирующим действием с другой.
В этом исследовании использовали CaHA-КМЦ (Radiesse). Перед проведением испытаний готовили образцы CaHA-КМЦ в различных разведениях. Объем физиологического раствора для приготовления соответствующих разведений неразведенного препарата, а именно 1:0,25; 1:0,5; 1:1; 1:2 и 1:3, составлял 0; 0,38; 0,75; 1,5; 3 и 4,5 мл соответственно.
Результаты показали, что различные разведения CaHA охватывали весь диапазон значений G″ филлеров на основе ГК, при этом минимальное значение G″ (1:3) составляло ~ 1 Па, а максимальное значение G″ (неразведенный препарат) — 427 Па, таким образом, разница составляла 426 Па. Значения показателя tan δ позволяют сделать вывод, что во всех филлерах на основе ГК, неразведенном CaHA-КМЦ и CaHA-КМЦ в разведении 1:0,25 преобладают упругие свойства (tan δ < 1), а в CaHA-КМЦ в разведениях 1:0,5 и выше — вязкие свойства (tan δ > 1). Кроме того, у CaHA-КМЦ в высоких разведениях (> 1:1) исключительно высокие значения tan δ; это позволяет предположить, что он лишь в незначительной степени обладает упругими свойствами и в основном ведет себя подобно жидкому веществу.
Гель на основе CaHA-КМЦ в в высоком разведении (1:1 и более) проявлял преимущественно вязкие свойства со значениями tan δ более 1 и снижением модуля упругости на 98 %. Кроме того, высокие разведения геля на основе CaHA-КМЦ характеризовались снижением G″ на 95 % и G* на 97 %. При таких изменениях реологических показателей филлеры в высоких разведениях обладают минимальной когезивностью и свойствами, присущими жидким веществам, а значит, идеально подходят для биорегенерации тканей, но при этом не увеличивают объем. Иначе говоря, разведение филлера позволяет влиять на ожидаемый эффект — волюмизирующий или биостимулирующий.
CaHA-КМЦ отличается способностью оказывать прямой волюмизирующий эффект и биостимулирующее действие в континууме «упругость — регенерация». Результаты свидетельствуют о том, что реологические характеристики CaHA-КМЦ можно изменять в широком диапазоне значений вязкоупругих показателей путем титрования разведения — от высоких значений упругости до низких значений когезивности. С помощью изменения объема водного разведения можно выполнять модуляцию реологических характеристик CaHA-КМЦ, обеспечивая потенциальное соответствие диапазону значений реологических показателей филлеров на основе ГК и расширяя варианты клинического применения. Результаты исследования могут стать основой для дальнейших исследований потенциального использования модуляции реологических характеристик в клинической практике с учетом конкретных потребностей пациента и целей.
Узнать больше в приложении для врачей-косметологов Merz City.


