 16418
16418 16418
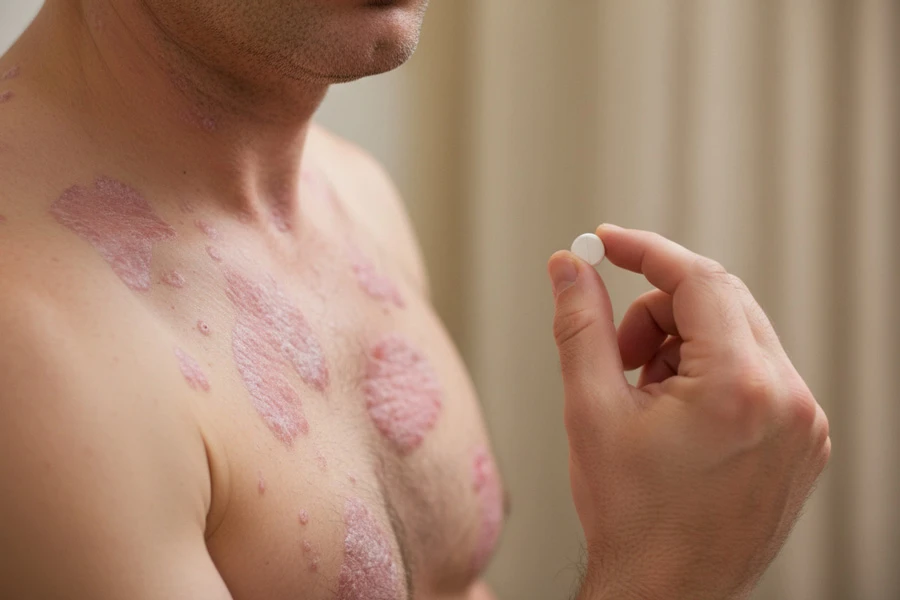
16418Японская фармкомпания Takeda создала препарат засоцитиниб для лечения бляшечного псориаза с использованием ИИ, препарат успешно прошел ключевые исследования III фазы.
Компания Takeda объявила о положительных результатах двух основных рандомизированных, многоцентровых, двойных слепых, плацебо- и активно-контролируемых исследований фазы III препарата зазоцитиниб (TAK-279). Это высокоселективный пероральный ингибитора тирозинкиназы 2 (TYK2) нового поколения. Препарат создан для лечения взрослых пациентов с бляшечным псориазом средней и тяжелой степени.
Исследования показали, что засоцитиниб при приеме один раз в день превосходит плацебо по основным конечным точкам: sPGA достигла 0/1, а PASI 75 к 16 неделе лечения. То есть врачи зафиксировали полное или почти полное очищение кожи у пациентов, кроме того, у всех состояние кожи улучшилось на 75% и более.
Выраженные улучшения врачи отметили уже на 4-й неделе терапии, они продолжали нарастать до 24-й недели. Исследования также подтвердили все 44 второстепенные конечные точки, в том числе PASI 90, PASI 100 и sPGA 0 по сравнению с плацебо и апремиластом.
«Результаты II фазы подтвердились в III фазе. Более чем у половины пациентов, принимавших засоцитиниб, кожа стала чистой или почти чистой (PASI 90), а у 30% кожа стала полностью чистой (PASI 100) на 16-й неделе лечения. И улучшения продолжали нарастать до 24-й недели», — добавил Энди Пламп, доктор медицинских наук, президент отдела исследований и разработок компании Takeda.
Пациенты в целом хорошо переносили засоцитиниб. Профиль безопасности и переносимости препарата соответствовал результатам предыдущих исследований. Наиболее частыми нежелательными явлениями в течение 24 недель были инфекции верхних дыхательных путей, назофарингит и акне. Новых сигналов о безопасности ученые не выявили.
Сейчас засоцитиниб проходит сравнительное исследование с деукравацитинибом (Deucravacitinib, тоже ингибитор TYK2) при лечении бляшечного псориаза, исследования III фазы при лечении псориатического артрита и исследования II фазы при лечении болезни Крона и язвенного колита, а также при других показаниях.
Takeda продемонстрирует результаты на предстоящих медицинских конгрессах. В 2026 финансовом году компания планирует подать заявку на регистрацию нового препарата в FDA и другие регулирующие органы.

