Кожа отражает возраст, и, следовательно, одним из этапов антивозрастного процесса является ее омоложение. Внутренние и внешние процессы старения кожи имеют схожие молекулярные механизмы, например, активные формы кислорода влияют на способность фибробластов продуцировать все компоненты внеклеточного матрикса, тем самым усиливая признаки старения. Первый признак старения может быть вызван и отсутствием гиалуроновой кислоты (ГК).
Гиалуроновая кислота является основным гликозаминогликаном, присутствующим в организме, особенно в коже, соединительной ткани и стекловидном теле глаза . Примерно 50 % запасов ГК в организме находится в коже. ГК представляет собой чрезвычайно гидрофильную молекулу, которая способна удерживать вес воды, в сто раз превышающий собственный вес молекулы. При более низких концентрациях ГК обмен ускоряется. Кроме того, ГК функционирует в рамках формирования кровеносных сосудов и каркаса, через который происходит миграция клеток, заживление ран и восстановление тканей. ГК также обладает способностью растягивать фибробласты и стимулировать выработку коллагена и тубулина2.
Внеклеточный матрикс (substantia intercellularis) – это комплекс коллагена, гликопротеинов и протеогликанов. Белки выполняют несколько функций. Одна из основных – взаимодействие с компонентами соединительной ткани через взаимодействие с клеточными рецепторами – интегринами, которые инициируют межклеточные контакты, взаимодействуют с факторами роста, секретируемыми при повреждении тканей. Фибробласты продуцируют кислые мукополисахариды – основной компонент межклеточного вещества соединительной ткани (гиалуроновую кислоту, хондроитинсерную кислоту, глюкозамин, галактозамин)3.
Особый интерес представляют клетки фибробластического ряда – именно они являются преобладающей популяцией клеток рыхлой волокнистой соединительной ткани и занимают одно из ключевых мест при ее формировании.
Следующие клетки относятся к дифферону фибробластов: прогениторные клетки фибробластического ряда, малодифференцированные фибробласты, дифференцированные или зрелые клетки, или собственно фибробласты, миофибробласты; малоактивные клетки (так называемые фиброциты), фиброкласты.
Основной источник фибробластов – малодифференцированные фибробласты. Под действием стимуляции эти фибробласты могут пролиферировать и генерировать новые фибробласты. Локальный эпителиально-мезенхимальный переход – это центральный механизм дифференцировки клеток при формировании органов и тканей. Однако ряд исследователей считает, что фибробласты могут образовываться при помощи данного механизма и во взрослом организме при воспалении или тканевом повреждении. Циркулирующие прогениторные клетки фибробластического ряда имеют маркеры как у лейкоцитов (CD45+, LSP-1), так и моноцитов (CD11a+, CD11b+, CD13+, CD32+, CD64+) и прогениторных клеток (CD34+, CD105+), а также экспрессируют продукты, присущие фибробластам (коллаген I типа, фибронектин, виментин, матричную металлопротеазу-9). В ответ на стимуляцию IL-1β прогениторные клетки секретируют провоспалительные цитокины (TNF, IL-6, IL-8, IL-10) и металлопротеазу-9. Прогениторные клетки фибробластического ряда способны также секретировать проангиогенные факторы – вазоэндотелиальный фактор роста, тромбоцитарный фактор роста (PDGF) AA, макрофагальный колониестимулирующий фактор, фактор роста гепатоцитов, гранулоцитарномакрофагальный колониестимулирующий фактор (GM-CSF), основной фактор роста фибробластов (FGF2), трансформирующий фактор роста (TGF).
Внимание ученых привлекает еще одна разновидность клеток фибробластического ряда – миофибробласты. Они были описаны на основании морфологических признаков как фибробласты, имеющие некоторые признаки гладкомышечных клеток, так как способны синтезировать гладкомышечный актин. Миофибробласты имеют цитоплазматические актиновые микрофиламенты, часто образуют синцитии. Считают, что эта клетка по своей дифференцировке лежит между фибробластами и гладкомышечными клетками. Они играют важную роль в регуляции таких фундаментальных процессов, как подвижность, пролиферация, дифференцировка, апоптоз, репарация тканей, воспаление и иммунный ответ. Индуцируют активацию и пролиферацию миофибробластов многие цитокины (IL-1, IL-4, IL-6, IL-8), факторы роста (TGF-α, TGF-β, EGF (эпидермальный фактор роста), GM-CSF, PDGF-AA, PDGF-BB, FGF1, FGF2, IGF-I (инсулинподобный фактор роста-I), IGF-II, а также альдостерон, тромбин, ангиотензин II, эндотелин. При этом наиболее выраженным активирующим эффектом обладает TGF-β. Источником TGF-β в поврежденной ткани могут быть лейкоциты, клетки паренхимы и эпителия, а также сами миофибробласты. PDGF отвечает за пролиферацию миофибробластов. Миофибробласты играют ключевую роль в заживлении раны. В течение репаративного процесса они выделяют цитокины, эйкозаноиды, NO, факторы роста, а также секретируют коллаген и другие белки внеклеточного матрикса. Миофибробласты активируются после повреждения ткани. В ответ на провоспалительные цитокины, секретируемые поврежденными эпителиальными клетками и лейкоцитами, миофибробласты начинают секретировать белки внеклеточного матрикса и факторы роста. После завершения процесса репарации они подвергаются апоптозу5.
Гиалуроновая кислота создает интерфейс между волокнами коллагена и эластина и, таким образом, заполняет внеклеточный матрикс, улучшает механическую поддержку в коже и удаляет свободные радикалы4. При достаточном уровне ГК кожа здоровая, эластичная, наполненная, сохраняет молодость, внешний вид, но ГК постоянно «переворачивается» в организме и разлагается внутри лизосом под действием гиалуронидаз, кодируемых генами HYAL1 и HYAL2.
Процесс производства ГК – сложный биохимический каскад, управляемый различными ферментами и кофакторами. Включает факторы роста TGF-β1, FGF1, гиалуронансинтазы (HAS1, HAS2, HAS3) – ферменты, синтезирующие молекулы ГК, и мембранный рецептор CD44. В производстве ГК при определенных обстоятельствах могут участвовать и фибробласты.
В зависимости от молекулярного размера синтезируемых молекул ГК различают три типа HAS – HAS1, HAS2 и HAS3. HAS2 синтезирует молекулы большого размера ГК (2 × 106 Да); следовательно, он играет важную роль в синтезе ГК в фибробластах, миофибробластах и, что наиболее важно, в самой дерме, тогда как HAS1 облегчает образование как больших, так и малых молекул, синтезированных по HAS3.
Трансформирующий фактор роста бета 1 (TGF-β1) главный регулятор биосинтеза во внеклеточном матриксе на протяжении всей активации сигнальных путей, которые регулируют ЕСМ гены и индуцируют выработку коллагена, фибронектина и эластина в дерме. Сигнальный путь TGF-β необходим для поддержания структурной и механической интеграции кожной соединительной ткани за счет увеличения производства ЕСМ. TGF-β1контролирует пролиферацию и дифференцировку клеток.
Кислый фактор роста фибробластов 1 (FGF1) играет роль в регенерации и пролиферации клеток фибробластов, которые продуцируют коллаген и эластин, а также приводит к экспрессии HAS и синтезу ГК.
При взаимодействии с ГК активируются некоторые биологические процессы, такие как эндоцитоз, миграция клеток, дифференцировка (специализация) и пролиферация (образование клеток). Основным рецептором ГК является CD44. ГК в сочетании с CD44 способствует подтяжке кожи, увлажнению, CD44 также регулирует экспрессию белков.
Истощение запасов гиалуроновой кислоты в настоящее время корректируется с помощью омолаживающих увлажняющих средств, кремов от морщин или инъекций, содержащих ГК и витамины. Биоревитализация стала золотым стандартом для повышения увлажненности тканей. Во время процедуры гиалуроновая кислота различной концентрации вводится в глубокие слои кожи, создавая депо вещества. Однако описанные методы непосредственно доставляют ГК или витамины в ткани кожи и заменяют функции фибробластов, но не способны восстановить естественную способность производить ГК. Вещество поступает извне, а не синтезируется в самом организме.
Практика последнего времени – использование радиочастотной (РЧ) и ультразвуковой (УЗ) энергии по отдельности с целью восстановления синтеза ГК, однако, было обнаружено, что подобные методы стимулируют и выработку коллагена и эластина.
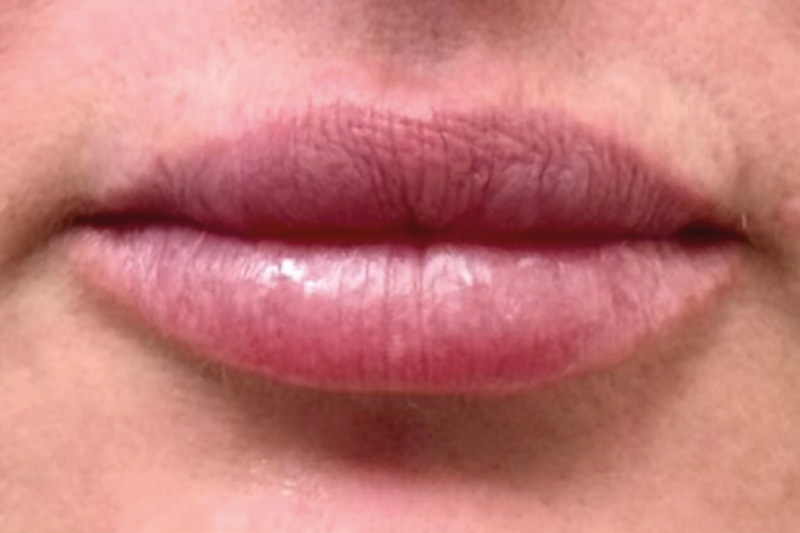
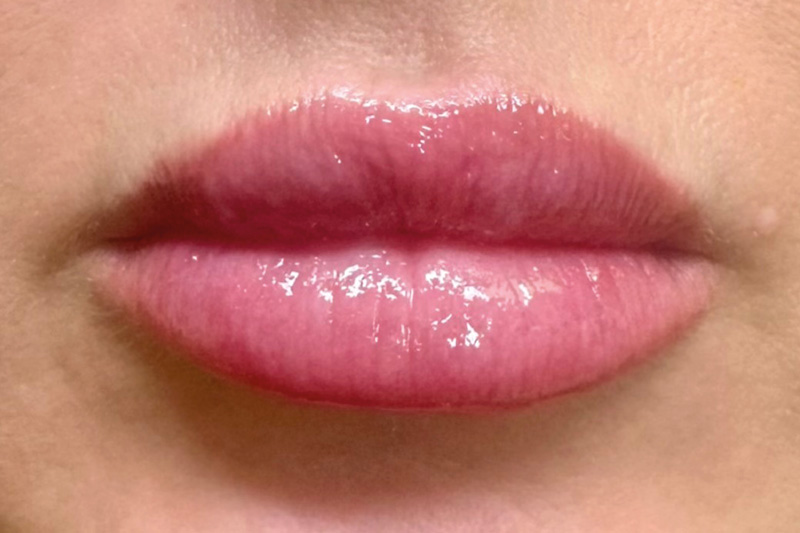
С точки зрения возможностей пролиферации органспецифических клеточных элементов все органы и ткани могут быть классифицированы на три группы:
При повреждении тканей и органов первой группы возможно полное восстановление поврежденных тканей, ткани второй и третьей группы из-за ограниченных способностей к регенерации способны восстанавливаться через развитие грануляционной соединительной ткани с формированием на месте повреждения соединительнотканного рубца. Поэтому соединительная ткань как элемент репаративного процесса многие годы привлекает пристальное внимание. В последние годы в связи с бурным развитием знаний в области молекулярной и клеточной биологии внимание фокусируется в том числе на возможности управления ростом и развитием соединительной ткани5. Новая технология Exion, созданная BTL Industries одновременно излучает монополярный радиочастотный сигнал и направленный ультразвук (TUS), чтобы использовать преимущества синергетического эффекта обеих технологий при одновременном применении1.
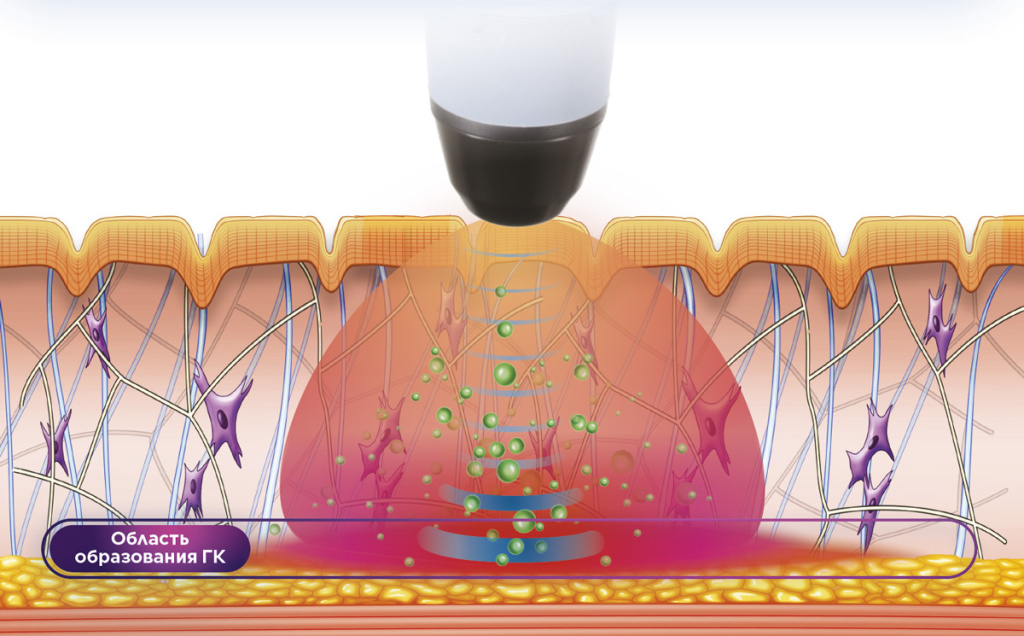
Исследования продемонстрировали, что влияние теплового и механического стресса на метаболизм фибробластов создавало благоприятные условия для синтеза ГК2. Радиочастотное излучение вызывало повышение температуры путем подачи осциллирующего электрического тока на обрабатываемую ткань, где это приводит к столкновениям между заряженными молекулами и ионами, кинетическая энергия превращается в тепло. Ультразвуковые механические волны с частотой 22–30 кГц, 1 МГц и 3 МГц представляет собой волну механического сжатия, которая стимулирует ткани как с помощью механических, так и термических механизмов.
Хотя оба метода способствуют обеспечению тепловых и механических напряжений, TUS фокусируется аналогично тому, как увеличительное стекло фокусирует свет, создавая меньшую, но концентрированную область воздействия, что позволяет обеспечить более глубокое и точное прицеливание. При этом не возникает нежелательных эффектов в ретикулярной дерме, месте с наиболее активными дермальными фибробластами. Они механически стимулируются, что приводит к дополнительным термическим приращениям и слабым внутриклеточным колебаниям в этом слое1. Кроме того, механическое воздействие TUS, такое как акустическое микропотоковое движение, также способствует стимуляции восстановления фибробластов и последовательному производству ГК, синтезу коллагена и регенерации тканей, что приводит к улучшению качества кожи и более молодому внешнему виду3.
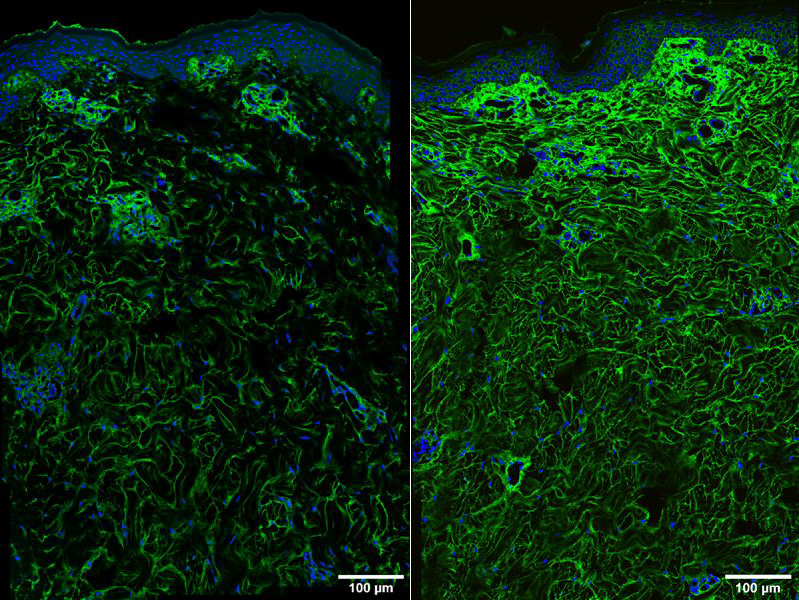
В процессе процедуры с использованием ультразвука на ткани производится комплексное механическое, тепловое и биологическое воздействие, а также создается физико-химический эффект. Звуковые волны создают разницу давлений, увеличивая проницаемость клеточных мембран и улучшая микроциркуляцию в клетках эпидермиса и дермы, происходит ускорение клеточного метаболизма. Благодаря механическому воздействию ультразвука процесс поступления в организм кислорода и питательных веществ значительно улучшается5.
Исследование Duncan et al. 2024 показало, что под действием Exion производство HAS1 и HAS2 достигало пика после лечения, причем HAS1 и HAS2 показали увеличение на 98 и 45 % соответственно, их производство медленно снижалось при наблюдении через 1 и 2 месяца. Измерения при помощи матричной лазерной десорбции (MALDI) и времяпролетной камеры (TOF) показали, что использование Exion повысило выработку собственной гиалуроновой кислоты на 224 %1.
Сочетание монополярного радиочастотного сигнала и направленного ультразвука в технологии Exion в виде одномоментной подачи и синхронизации двух энергий может быть показано для активации синтеза ГК в коже.


